Prerequisiti:
Il Cloro è un gas del gruppo VII (alogeno), è più pesante dell'aria e possiede un colore verde. Non è presente libero in natura.
Obbiettivo:
Osservazione dei comportamenti del Cloro.
Materiali:
- Beuta
- Acido cloridrico (o muriatico)
- Permanganato di potassio
- Filo di rame
- Filo di ferro
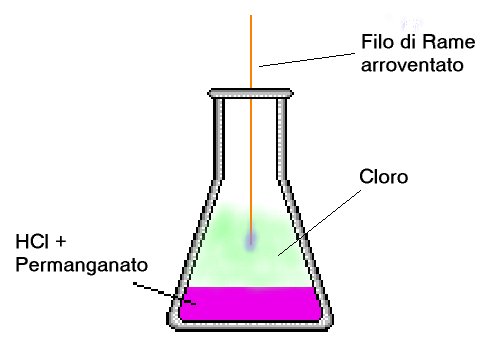 Versare nella beuta una piccola quantità di permanganato, aggiungere 20 cc di acido cloridrico; la miscela produrrà un gas che tende dal viola al nero. Scaldare su una fiamma l'estremità del filo di rame nudo, inserirlo nella beuta SENZA immergerlo nel liquido, fare lo stesso procedimento con il filo di ferro.
Versare nella beuta una piccola quantità di permanganato, aggiungere 20 cc di acido cloridrico; la miscela produrrà un gas che tende dal viola al nero. Scaldare su una fiamma l'estremità del filo di rame nudo, inserirlo nella beuta SENZA immergerlo nel liquido, fare lo stesso procedimento con il filo di ferro.Conclusioni:
Filo di Rame
Il filo diventerà rapidamente incandescente e si consumerà per la formazione di cloruro di rame dalla reazione diretta tra metallo e cloro.
Filo di Ferro
Il filo di ferro brucerà, producendo un fumo arancione costituito da cloruro ferrico.

